- Субекти
- Обобщение
- Въведение
- Методи
- Химически продукти
- Животни
- Анализ на аортната съдова реактивност
- Анализ на мезентериалната съдова реактивност
- Клетъчна култура
- Уестърн блотинг
- Хистология
- Статистика
- Резултати
- Ефекти на PVAT върху реактивността на аортата
- Ефект на PVAT върху реактивността на мезентериалната артерия
- HFD намалява активността на eNOS
- Ремоделиране на аорти и PVAT при плъхове в HFD
- Експресия на AMPK и mTOR в аорти на плъхове в HFD
- Ефект на PVAT върху експресията на AMPK/mTOR в култивиран VSMC
- Дискусия
Субекти
- Клетъчна сигнализация
- Мазнини
- Затлъстяване
- Съдови заболявания
Обобщение
Методи
Химически продукти
Фенилефрин (PE), ацетилхолин (ACh) и нитроглицерин (NTG) са закупени от Sigma-Aldrich (Taufkirchen, Германия).
Животни
Мъжки плъхове Wistar, на възраст от 6 до 8 седмици, са получени от Charles River (Sulzfeld, Германия). Плъховете са настанени в условия 12/12 h ден/нощ и на всички животни е дадена храна и вода ad libitum. Местният комитет за грижи и употреба на животните одобри всички процедури за грижи и употреба на животните. Изследването отговаря на Ръководството за грижа и използване на лабораторни животни, публикувано от Националния здравен институт на САЩ (NIH Publication No. 85-23, ревизиран 1996 г.). Животните са получавали стандартна хранителна диета (контролна група, n = 18) или HFD (HFD група, n = 18) в продължение на 6 месеца.
Анализ на аортната съдова реактивност
Анализ на мезентериалната съдова реактивност
Клетъчна култура
VSMC се получават от гръдни аорти на плъхове и се култивират, като се използва методът на тъканна експлантация, както е описано по-рано от нашата група. 27 периваскуларни адипоцити са получени от периаортна мастна тъкан и са култивирани, като се използва методът на тъканна експлантация, както е описано по-горе. 28 VSMC/адипоцитни кокултури са установени в присъствието или отсъствието на 10 μM съединение С, инхибитор на AMPK (Calbiochem, Сан Диего, Калифорния, САЩ), както е описано по-рано от противоположните страни на културните пластмасови вложки от порест полиетилен терефталат, който е имал ефективна културна площ от 0,3 cm 2, размер на порите 0,4 μm и плътност на порите 1 × 108 на cm 2 (Becton Dickinson, Franklin Lakes, NJ, USA).
Уестърн блотинг
Хистология
Дебелината на аортната туника се определя съгласно установените техники. 29 Аортната тъкан беше фиксирана в 10% физиологичен разтвор, буфериран с формалдехид/фосфат и вградена в парафин. След рутинни хистологични процедури напречните сечения, проксимални до първата междуребрена артерия, бяха оцветени с Victoria Blue и Ponceau S и бяха изследвани при увеличение × 200. Изображенията бяха получени с цифров фотоапарат с помощта на микроскоп Nikon TE2000 (Nikon Corporation, Tokyo Japan). Средата на туниката беше определена като областта между вътрешните и външните еластични пластини, които бяха измерени в четири ортогонални точки на артериалните секции по време на три последователни аортни пръстена на животно с помощта на софтуера за изображения NIS-Elements 3.0 (Nikon Corporation).
Размерът на периаортната адипоцит е измерен, както е описано по-горе. 30 периаортни мастни тъкани бяха събрани от шест плъха, фиксирани с 10% буфериран формалин, вградени в парафин и оцветени с хематоксилин и еозин. Изображенията бяха заснети с помощта на микроскоп Nikon TE2000 (Nikon Corporation) и площта за общо 100 адипоцити, извлечени от всеки плъх, беше определена с помощта на софтуера за изображения NIS-Elements 3.0 (Nikon Corporation).
Статистика
Данните са средни ± sem. Полумаксималната ефективна концентрация на агонист (EC50) и максималният отговор (E max) са изчислени от индивидуалните криви на концентрация-отговор на агонист, използвайки GraphPad Prism 3.0 (Сан Диего, Калифорния, САЩ). Статистическите разлики в средните стойности бяха оценени с помощта на t-тест на Student или еднопосочен дисперсионен анализ с многократни сравнителни post hoc тестове на Bonferroni, според случая. Двустранните P-стойности под 0,05 се считат за статистически значими.
Резултати
Ефекти на PVAT върху реактивността на аортата
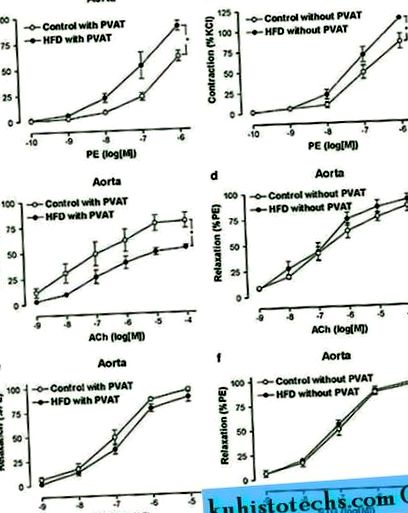
В сравнение с плъховете на хранена храна, телесното тегло и масата на мастната тъкан са значително увеличени при плъхове на HFD за 6 месеца (Таблица 1). Въпреки това, систолното кръвно налягане на маншета на опашката не се различава между двете групи (127 ± 4 mm Hg при HFD срещу 123 ± 5 mm Hg при диетата на Chow, P> 0,05). Индуцираната от PE съкратителна реакция на аортните пръстени беше значително увеличена при HFD-хранени плъхове, особено в присъствието на PVAT (Фигури 1а и b) (Таблица 2). Освен това, зависимата от ендотел релаксация е значително намалена при плъхове с HFD в сравнение с плъхове на хранителна диета само в присъствието на PVAT (Фигури 1в и d) (Таблица 2). Независимо от това, независимото отпускане на ендотела не е било засегнато в присъствието или отсъствието на PVAT при плъхове, нито с диета на Чоу, нито с DCA (Фигури 1д и f) (Таблица 2).
Таблица в пълен размер
Ефекти на PVAT върху реактивността на аортата. PE-индуцирано свиване ( да се, б ) и релаксация, причинена от ACh или NTG ( ° С - F ) са изследвани в прясно изолирани аортни пръстени със или без PVAT от плъхове, поставени на контролна и високомаслена диета (HFD). Резултатите са средните ± sem от 6 до 8 пръстена от 6 до 8 плъхове на група. * Р
Ефект на PVAT върху реактивността на мезентериалната артерия. PE-индуцирано свиване ( да се, б ) и релаксация, причинена от ACh- ( ° С, д ) или NTG ( и, F ) бяха изследвани в прясно изолирани мезентериални артериални пръстени в присъствието или отсъствието на тяхната периаортна мастна тъкан. Резултатите са средно ± sem от 5-10 пръстена от 5-10 плъха на група; * Р
Експресия на ENOS и фосфорилиране в аортата. Общо eNOS и p-eNOS Ser1777 в аортната тъкан от плъхове, хранени с (chow-) или HFD, бяха открити чрез Western blotting. Стълбовидните графики показват относителното фосфорилиране, нормализирано към контролната група. Резултатите са средно ± sem от 4-8 независими експеримента с 4-8 плъхове. ** P 2, съответно P
Ремоделиране на аортата и PVAT при плъхове в HFD. ( да се ) Изображенията показват разрези на аорти, оцветени с Виктория синьо и Понсо S от всяка група плъхове. Ляв панел, контролна група; десен панел, HFD група. Скалата показва 100 µm; увеличение, × 200. ( б ) Графиката показва количественото определяне на дебелината на туниката. Резултатите са средни стойности ± sem (n = 3 плъхове на група). ** P ** P 31 AMPK експресията и фосфорилирането в аортите на плъхове при HFD са значително намалени в сравнение с тези на хранителна диета (Фигура 5а). Както е показано в представителните ленти, нивата на общия и фосфорилиран mTOR се повишават значително с HFD захранването (Фигура 5b). Съотношението на фосфорилирания mTOR към общия mTOR обаче не се променя (Фигура 5b). Освен това, експресията на протеина PI3K и Akt и фосфорилирането в аортата са сходни в двете групи (Фигури 5в и г).
Експресия и фосфорилиране на AMPK, mTOR, PI3K и Akt протеини в аортната тъкан. AMPK/p-AMPK Thr172 ( да се ), mTOR/p-mTOR Ser2448 ( б ), PI3K/p-PI3K ( ° С ) и Akt/p-Akt ( д ) в аортна тъкан с чау- (контрол) или HFD-хранене.Плъховете са открити чрез Western blotting. Стълбовидните графики показват относителното фосфорилиране, нормализирано към контролната група. Резултатите са средно ± sem на 4-8 независими експеримента на 4-8 плъхове. ** Р
Въпреки че при спонтанно хипертонични плъхове е съобщено намаляване на контракционния ефект на периваскуларната мастна тъкан върху мезентериалните артериоли, 5 малко проучвания са изследвали ролята на PVAT при затлъстяването. Това проучване показва за първи път, че наличието на PVAT нарушава релаксацията както в проводящата артерия, така и в малките артериоли при индуцирани от HFD плъхове със затлъстяване. Освен това плъховете със затлъстяване в HFD имат по-големи адипоцити в PVAT и по-дебела аортна туника. Като се имат предвид тези нови открития, решихме да проучим основните механизми, които са в основата му.
AMPK е член на семейство на метаболит-чувствителни протеинкинази, присъстващи във всички еукариоти и се смята, че регулира клетъчната пролиферация в отговор на енергийния статус или наличието на хранителни вещества. mTOR, еволюционно запазена серин/треонин киназа, интегрира хранителни и митогенни сигнали за регулиране на клетъчния растеж и клетъчното делене чрез протеин транслация/синтез. Активирането на AMPK потиска mTOR сигнализирането и увеличава активността на TSC1-TSC2 комплекса. 38 Тези открития предполагат, че AMPK активирането инхибира mTOR активността, за да ограничи синтеза на протеин. NO играе критична роля в модулирането на съдовата релаксация, а активността на ензима, отговорен за производството на NO, eNOS, се регулира от редица протеинкинази, включително AMPK. 21 AMPK е необходим за адипонектин, тромбин и индуцирано от хистамин фосфорилиране на NOS и последващо ендотелно производство на NO. двадесет и едно
Настоящите резултати показват, че при HFD-индуцирани затлъстели аорти на плъх, нивата на AMPK и p-eNOS са понижени, докато mTOR експресията се увеличава. Освен това, инкубацията на култивиран VSMC с PVAT намалява експресията на AMPK и увеличава mTOR експресията. Нашите резултати подкрепят схващането, че ненормален AMPK/mTOR сигнален път може да е отговорен за HFD-индуцирана съдова дисфункция и ремоделиране при затлъстели плъхове. Освен това, инхибиторният ефект на съединение С върху индуцираното от културата увеличаване на mTOR фосфорилирането допълнително потвърждава, че mTOR се регулира от PVAT чрез AMPK активиране.
Патофизиологичният механизъм, чрез който PVAT може да медиира съдова дисфункция и ремоделиране, не е напълно изяснен. Увеличеното производство на реактивни видове кислород, участващи в механизми, които насърчават ендотелната дисфункция и водят до съдово ремоделиране, се предлага като потенциален медиатор. Съобщава се, че PVAT индуцира провъзпалително състояние при HFD-индуцирани затлъстели мишки. 19 Възпалителната клетъчна инфилтрация в периваскуларната тъкан и следователно миграцията на възпалителни фактори към съдовата стена също могат да бъдат възможните механизми, които водят до съдова дисфункция и ремоделиране.
- Крушово тяло или ябълково тяло, това, което определя, че в някои области натрупваме повече мазнини, отколкото в други
- Ниска концентрация на мед, свързана с мастни мастни клетки
- Повишените мазнини в корема по време на бременност могат да предвестят диабет по време на бременност
- Внимавайте с диетата си, тялото се нуждае от мазнини Куриерът
- Колата; Уникално обучение за смесени бойни изкуства (ММА) P; Загуба на мазнини - MSN здраве и