Вижте статиите и съдържанието, публикувани в този носител, както и електронните резюмета на научни списания към момента на публикуване
Бъдете информирани по всяко време благодарение на сигнали и новини
Достъп до ексклузивни промоции за абонаменти, стартиране и акредитирани курсове
Неврологията е официалното списание на Испанското общество по неврология и от 1986 г. публикува научни публикации в областта на клиничната и експерименталната неврология. Съдържанието на неврологията варира от невроепидемиология, неврологична клиника, неврологично управление и помощ и терапия, до основни изследвания в неврологията, прилагани към неврологията. Тематичните области на списанията включват детска неврология, невропсихология, неврорехабилитация и неврогетриатрия. Статиите, публикувани в Neurology, следват процес на двойно сляпо преразглеждане, така че произведенията са подбрани според тяхното качество, оригиналност и интерес и по този начин са подложени на процес на усъвършенстване. Форматът на статията включва редакционни материали, оригинали, рецензии и писма до редактора, неврологията е средство за научна информация с признато качество при професионалисти, интересуващи се от неврология, които използват испански език, както се вижда от включването му в най-престижните и селективни библиографски индекси в света.
Индексирано в:
MEDLINE, EMBASE, Web of Science, разширен индекс за научно цитиране, предупредителни услуги и неврология, индекс за цитиране на неврология, ScienceDirect, SCOPUS, IBECS и MEDES
Следвай ни в:
Импакт факторът измерва средния брой цитати, получени за една година за произведения, публикувани в публикацията през предходните две години.
CiteScore измерва средния брой цитати, получени за публикувана статия. Прочетете още
SJR е престижна метрика, базирана на идеята, че всички цитати не са равни. SJR използва алгоритъм, подобен на ранга на страницата на Google; е количествена и качествена мярка за въздействието на дадена публикация.
SNIP дава възможност за сравнение на въздействието на списанията от различни предметни области, коригирайки разликите в вероятността да бъдат цитирани, които съществуват между списанията на различни теми.
- Обобщение
- Ключови думи
- Резюме
- Ключови думи
- Обобщение
- Ключови думи
- Резюме
- Ключови думи
- Библиография
Чернодробната фиброза и нейният последен етап, цироза, представляват огромен глобален здравен проблем. Чернодробната енцефалопатия (HE) или портосистемната енцефалопатия е дългосрочно клинично състояние на цироза. Този преглед подчертава молекулярните основи на HD, както и ролята на оксидативния стрес в развитието на това заболяване.
Няколко проучвания показват, че HE е от многофакторен произход, промени в кръвно-мозъчната бариера, вещества като амоний и манган, както и промени в невротрансмисията на допамин, глутамат и GABA, са замесени в патогенезата на това заболяване.
HD е тежко усложнение както на остра, така и на хронична чернодробна недостатъчност. Невропатологично се характеризира с астроцитни промени, известни като астроцитоза на Алцхаймер тип II и с променена експресия на специфични астроцитни протеини, като глиален фибриларен киселинен протеин, глутамин синтетаза, инхибитори на моноаминооксидазата и периферни бензодиазепинови рецептори.
HD е сложен невропсихиатричен синдром, свързан с чернодробна недостатъчност. Тези промени са резултат от увеличаване на оксидативния стрес в мозъка като последица от действието на невротоксините. Основната стратегия за лечение на НЕ е насочена към намаляване на амоняка, или чрез намаляване на неговото усвояване/производство, или насърчаване на неговото елиминиране.
Чернодробната фиброза и нейният краен стадий, цироза, е огромен световен здравен проблем. Чернодробната енцефалопатия (HE) или портално-системната енцефалопатия продължава да бъде основен клиничен проблем на дългосрочната цироза. В този преглед ние наблягаме на молекулярната основа на НЕ и участието на оксидативен стрес в развитието на това заболяване.
Няколко проучвания предполагат, че патогенезата на НЕ може да бъде многофакторна и да е свързана с различни фактори, като промени в кръвно-мозъчната бариера, вещества; като амоняк и манган, невротрансмисионни нарушения като допамин, глутамат и GABA.
HE е тежко усложнение както на остра, така и на хронична чернодробна недостатъчност. Невропатологично се характеризира с астроцитни промени, известни като астроцитоза на Алцхаймер тип II. В допълнение, астроцитите проявяват изменена експресия на специфични за астроцитите протеини, като глиален фибриларен киселинен протеин, глутамин синтетаза, моноаминова оксидаза и бензодиазепинови рецептори от периферен тип.
HE е сложен невропсихиатричен синдром, свързан с чернодробна недостатъчност. Тези промени са резултат от повишаване на оксидативния стрес в мозъка поради невротоксинова активност. Основната стратегия за лечение на HE е насочена към намаляване на амоняка, което може да бъде постигнато или чрез намаляване на неговата абсорбция/производство или чрез увеличаване на отстраняването.
Клинични степени на чернодробна енцефалопатия.
| I степен | Липса на осъзнатост, еуфория или безпокойство и намалена продължителност на вниманието |
| Степен II | Летаргия, апатия, минимална дезориентация на времето и пространството, промени в личността и неподходящо поведение |
| III степен | Сънливост, объркване и дезориентация |
| IV степен | Яжте |
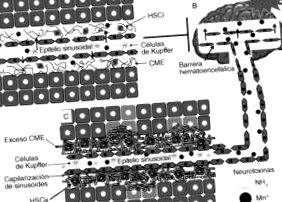
Патогенезата на HD включва действието на невротоксини като амоний и манган, в допълнение към различни явления, които включват промени в невротрансмисията, пропускливостта на кръвно-мозъчната бариера или енергийния метаболизъм (фиг. 2). Въпреки че патогенезата на HD е сложна и все още не е напълно разбрана, многобройни животински модели са използвани за изследване на развитието на това заболяване. Освен това появата на съвременни техники на клетъчната и молекулярна биология, както и използването на образни техники в неврофизиологията, позволи значителен напредък в разбирането на патогенезата на HE 16 .
Промени в развитието на чернодробна енцефалопатия. Нормалната мозъчна функция зависи в няколко отношения от нормалното функциониране на черния дроб. Въпреки че мозъкът е защитен от невротоксични вещества чрез кръвно-мозъчната бариера (характеристика на кръвоносните съдове в мозъка, която предотвратява преминаването на много съединения от кръвта в мозъчната тъкан), някои невротоксини могат да проникнат през тази бариера след нараняване на черния дроб. като цироза. Това чернодробно заболяване предизвиква увеличаване на невротоксичните вещества като амоний и манган, които от своя страна индуцират оксидативен стрес чрез преминаване на кръвно-мозъчната бариера, причинявайки увреждане на невротрансмисията, неуспех в синтеза на енергия и накрая клетъчна смърт.
Астроцитите заемат около една трета от обема на мозъчната кора и образуват сегрегационна бариера за невроните във външната среда. Те участват в различни процеси, важни за мозъчната функция, поддържат и регулират извънклетъчната среда, участват в усвояването на свободните радикали, задържането на метали, модулацията на имунния отговор и възпалението и влияят върху невронната възбудимост и невротрансмисия. Тези клетки представляват различни морфологични промени.По време на чернодробна цироза възниква астроцитоза на Алцхаймер тип II и при остра чернодробна недостатъчност астроцитите придобиват вид на подути клетки. Документирано е, че при HD астроцитите представят променена експресия на специфични астроцитни протеини, като глиален фибриларен киселинен протеин (GFAP), ензими като глутамин синтетаза (GS), инхибитори на моноаминооксидазата (МАО) и периферни бензодиазепинови рецептори (PBR) 19. .
Роля на астроцитите
Сред различните видове клетки в централната нервна система (ЦНС) астроцитите са важен източник на извънклетъчни протеини и адхезионни молекули. Те играят централна роля в образуването на глиални белези след множество форми на нараняване, за да запазят целостта на тъканите и да очертаят зоната на нараняване, в процес, наречен реактивна астроглиоза. Глиалният белег около лезията се опитва да спаси здравата тъкан на ЦНС от вторични лезии; но в същото време той инхибира възможната аксонална регенерация след нараняване 20 .
Роля на невроните
За разлика от морфологичните промени, описани в астроцитите, невроните не показват промени в клетъчната си архитектура по време на HD. При хистопатологични проучвания на мозъка при пациенти с хронично увреждане на черния дроб невроните се наблюдават в нормални условия и количества и някои маркери за невронна цялост като N-ацетиласпартат не се променят при тези пациенти. Изследванията върху животински модели на HD осигуряват убедителни доказателства, че механизмите на невронната смърт са подобни на тези, наблюдавани при исхемия. Тези механизми включват медиирана от NMDA рецепторна екситотоксичност, оксидативен/нитрозативен стрес, лактатна ацидоза и наличието на провъзпалителни цитокини. .
Амоний. Амонийът (NH3) е ключовият невротоксин, участващ в патогенезата на HD. През последните години беше постигнат важен напредък за определяне на неговата роля в генезиса на мозъчен оток по време на фулминантна чернодробна недостатъчност 13,22,23. Използването на амониеви инфузии при плъхове показва, че мозъчният оток и вътречерепната хипертония могат да бъдат предизвикани експериментално и че това явление може да бъде инхибирано с приложението на метоксимин сулфат, инхибитор на GS. Това доведе до концепцията, че глутаминът, получен от ЦНС, участва в амониевата детоксикация, като произвежда осмотичен градиент през кръвно-мозъчната бариера, което води до мозъчен оток и подуване на астроцитите 11,22. Структурните и неврохимични промени в мозъка в резултат на излагане на амоняк са обект на интензивни изследвания. Амонийът предизвиква астроглиални промени, които допринасят за подуване на клетките чрез увеличаване на вътреклетъчния глутамин, което води до промени в кръвно-мозъчната бариера, които влияят на глутаматергичната невротрансмисия и увеличават експресията на невронална азотна синтетаза 22 .
Дисфункция на допаминергичната невротрансмисия
Механизмът на намаляване на DA в HD се счита за причина за натрупването на фалшиви невротрансмитери. Увеличеното преобразуване на DA при пациенти с енцефалопатия повишава концентрацията на ароматните аминокиселини фенилаланин и тирозин в мозъка, и двата предшественика на невротрансмитера DA. Освен това е описано, че Mn 2+ променя допаминергичното предаване чрез увеличаване на DA конверсията. .
Глутаматът е аминокиселина и един от аминокиселинните невротрансмитери в мозъка с възбуждащ ефект. По принцип той се състои от централен въглероден атом, прикрепен към карбоксилна група (COOH) и амино група (NH 3). Мозъчният глутамат се получава само от ендогенни източници; главно от кетоглутарат, продукт от цикъла на Кребс 37. Невроналният глутамат действа като невротрансмитер по време на комуникация между невроните. Тези неврони могат да бъдат възбуждащи или инхибиторни. Възбудителното действие на глутамата в мозъка и гръбначния мозък на бозайниците е известно от 50-те години на миналия век, 37 но едва в края на 70-те години глутаматът е признат за основен предавател на възбуждане в нервната система при гръбначните животни 38 .
Гама-аминомаслената киселина (GABA) е преобладаващият инхибиторен невротрансмитер в ЦНС на бозайниците. Промяната на GABAergic невротрансмисията е замесена в патофизиологията на няколко неврологични и невропсихиатрични заболявания като епилепсия, шизофрения, невродегенеративни заболявания, нарушения на съня и чернодробна енцефалопатия. GABAergic невротрансмисията се медиира от GABA, който активира постсинаптичния GABA A рецепторен комплекс (GRC), специфичен лиганд на хлорид-селективни йонни канали, след активирането каналът се отваря и позволява на хлорида да влезе, за да инхибира постсинаптичния неврон. Промяната на GABAergic невротрансмисията в HD беше предложена преди повече от две десетилетия 39 .
Лечение на чернодробна енцефалопатия
Лекарства, използвани за лечение на чернодробна енцефалопатия.
- Ключови аспекти на кучешкия хроничен бронхит - Ateuves, за ветеринарния асистент
- 10 съвета за облекчаване на ци; етика
- Хранене на кон важни аспекти - TUXE Life
- Хирургия; a и Est Medicine; tica в Барселона, Granollers и Reus Cl; единична С; nons Терапия за тяло
- ° С; как да разберем резултатите от анален анализ; женска хормонална етика