Написано на 03 февруари 2020 г.
Индекс на статията
- Ендометриално-маточен рак
- епидемиология
- Рискови фактори
- Наследствен рак на матката
- Патологична анатомия и молекулярна биология
- Знаци и симптоми
- Диагноза
- Постановка
- Прогностични фактори
- Лечение
- Последващи действия
- Всички страници
АВТОР: Дра Луиза Санчес Лоренцо
Матката е кух мускулест орган с форма на обърната круша. Той се намира в женския таз пред ректума, зад пикочния мехур и в контакт с вагината. В горната му част от всяка страна влизат фалопиевите тръби.
Той е разделен на две части:
- Маточно тяло: съставено е от горните две трети и има две части: очното дъно (заоблена част над входа на фалопиевите тръби) и провлака (областта непосредствено над шийката на матката).
- Шийката на матката или шийката на матката, изпъкнала в горната част на вагината.
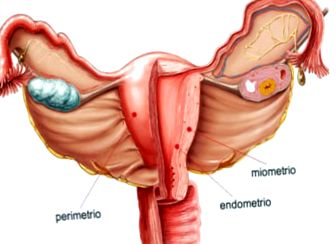
Стената на маточното тяло се състои от три слоя:
- Периметриум: външна серозна туника.
- Миометриум: tunica media, дебел слой гладка мускулна тъкан, който се разтяга по време на бременност. Тук са разположени основните съдове и нервите на матката.
- Ендометриум: вътрешна лигавична туника, която прилепва към миометриума. Тази подплата се подновява всеки месец след менструация.
Има доброкачествени лезии на матката, които трябва да се наблюдават за възможни усложнения. Миомите са доброкачествени тумори, които произхождат от мускулната стена на матката. Ендометриозата е наличието на ендометриална тъкан извън матката и може да представлява повишен риск за развитието на други тумори. Туморите на матката произхождат предимно от ендометриума поради промени в тези клетки.
Епидемиологични данни
В световен мащаб ракът на матката е седмото по честота новообразувание при жените и второто гинекологично новообразувание след рак на маточната шийка. През 2018 г. са диагностицирани 382 000 нови случая (8,4 случая/100 000 жени) и са регистрирани почти 90 000 смъртни случая (1,8/100 000 жени). В развитите страни това е най-често срещаният гинекологичен рак. Процентът на заболеваемост в тези страни представлява 14,7 случая/100 000 жени при смъртност 2,3/100 000 жени.
В Испания ракът на ендометриума е четвъртото по честота новообразувание при жени с 6784 нови случая през 2018 г., приблизително с честота от 13,7 случая/100 000 жени/година и смъртност от 3,6 случая/100 000 жени/година.
Средната възраст при поставяне на диагнозата е 63 години, но повече от 90% от случаите се диагностицират при жени> 50 години. 4% от пациентите са диагностицирани преди 40-годишна възраст.
75-80% от случаите се диагностицират в етап I с 5-годишна преживяемост от 90%. За съжаление 5-годишният процент на оцеляване е по-нисък, когато има регионално (68%) или отдалечено (17%) разпространение.
Рискови фактори
Повечето случаи не могат да бъдат предотвратени, но намаляването на рисковите фактори може да намали шанса за развитие на болестта.
Много е важно да осведомите всички жени за рисковите фактори и симптомите на рак на ендометриума.
РИСКОВИ ФАКТОРИ
Прекомерна експозиция на естрогени:
Възраст, средна възраст при диагноза 62 години.
-
Ако има фамилна анамнеза за роднина от първа степен (майка, сестра или дъщеря), рискът се увеличава от 50 години.
Предишна тазова лъчева терапия за друго новообразувание.
Наследствен рак на матката
Счита се, че от съвкупността от диагностицирани понастоящем рак на ендометриума, само 2-5% са наследствени, ако пациентът е бил диагностициран преди 50-годишна възраст, тази цифра се увеличава до 10%.
Популационният риск на жената от развитие на рак на ендометриума е приблизително 2%, но когато е свързан с наследствено-фамилен синдром, рискът му е между 3-50%.
Наследствените синдроми, най-често свързани с рака на ендометриума, са Sd на Lynch и Sd на Cowden, като последният е по-рядък, тъй като е по-рядък.
През последните години наследственият синдром на рак на гърдата и яйчниците (BRCA1/2) също се свързва с развитието на рак на ендометриума, особено при BRCA1, докато връзката с BRCA2 остава съмнителна. Други евентуално свързани наследствено-фамилни синдроми са Peutz-Jeghers Sd и Li-Fraumeni Sd.
Sd линч
BRCA 1/2
Sd cowden
Патологична анатомия и молекулярна биология
Класически класификацията на туморите е хистологична, но тъй като се придобиват нови знания на ниво молекулярна биология, можем да ги включим като допълнителна информация, която ще ни позволи да ги идентифицираме по-добре.
Хистологична класификация:
Той позволява стратифициране на туморите по броя на мутациите, като е в състояние да предскаже чувствителността към имунотерапия (antiPDL-1) и също така предоставя прогностична информация.
В клиничната практика се използват три имунохистохимични техники (p53, MLH1, MSH2, PMS2, MSH6) и една молекулярна техника (POLE мутации) с намерение да се направи приблизителна оценка.
ПОЛУ/ултрамутиран
(5-7%)
MSI/хипермутирано
(28-30%)
Номер на копие нисък
(39%)
Серозен/p53 абн
(23-26%)
Знаци и симптоми
- Ненормално генитално кървене: кардинален симптом (до 90% от случаите)
1. След 45 години.
Диагноза
Изправен пред който и да е от признаците и симптомите на подозрение, пациентът трябва да бъде насочен към гинекологичен кабинет за оценка.
1. Насочена анамнеза: съставяне на личните и семейните рискови фактори на пациента.
2. Гинекологичен преглед: инспекция със спекулум и колпоскопия, вагинално-абдоминален преглед, който ще позволи да се определи размерът на матката и ректо-вагинален преглед, за да се направи приблизителна оценка на размера на матката или ако инфилтрация на ректус-вагинален има съмнение за преграда и параметрия. Не забравяйте да опипате ганглийните територии.
3. Трансвагинален ултразвук: въвеждане през вагината на ултразвукова сонда, която позволява да се измери дебелината на ендометриума, граничната точка на дебелината обикновено се определя на 3 mm, което може да е различно в зависимост от това дали пациентът е пред- и постменопауза. Ако дебелината е по-голяма или има продължително гинекологично кървене, диагностичните тестове ще продължат.
4. Хистероскопия: представлява визуално изследване на шийката на матката и вътрешността на матката с тънка гъвкава тръба. Този тест може да има диагностични и терапевтични цели. Директният изглед на вътрешността на матката ни позволява да направим биопсия на всяка зона на съмнение, екстракция на полипи, миома или каутеризация на области на кървене. Може да се извършва със или без локална анестезия и е амбулаторна процедура.
5. Аспирационна биопсия на ендометриума: минимално инвазивна и амбулаторна техника, която позволява да се вземат слепи биопсии от лицата на матката и маточните ъгли. Висока чувствителност на специфичност при жени преди и след менопаузата.
6. Биопсия: вземане на малък фрагмент от ендометриума за потвърждаване на предполагаемата диагноза.
Ако диагнозата рак на ендометриума бъде потвърдена, ще бъдат поискани допълнителни тестове:
7. Туморни маркери: Обикновено се изисква CA125, променлива полезност в зависимост от вида на хистологията.
8. Ректоскопия и цистоскопия: позволяват директна визуализация на ректума и пикочния мехур съответно и ще се оценяват само когато има голямо съмнение за туморна инфилтрация.
9. Тестове за изображения:
да се. Тазовият магнитен резонанс (ЯМР): избор на тест за предоперативно стадиране, тъй като той е този, който най-добре оценява локарегионалното разширение на тумора, като представлява особен интерес дебелината на ендометриалната линия, наличието на маси в миометриума, степента на инфилтрация на миометриума, засягане или не на шийката на матката и оценка на увеличените аденопатии.
б. Компютърна томография (КТ): много полезна за оценка на лимфаденопатията и наличието на отдалечени метастази.
° С. PET-CT: по-голяма чувствителност от CT или MRI за откриване на метастази в лимфните възли. В момента, въпреки че е широко приет като част от първоначалното разширено проучване, основната му роля е в откриването на рецидиви или в лечението на локален рецидив.
Постановка
Постановката на тумора ни позволява ясно да определим неговия размер, местоположение, локално и далечно разширение (метастази). Правилното стадиране на тумора ни позволява да проектираме терапевтичната стратегия. Използваните две класификационни системи са TNM системата и FIGO системата, като последната е по-широко разпространена, но има връзка между двете. Последната актуализация на ендометриалната система FIGO е от 2009 г., като тази, която в момента използваме за класифициране на маточни карциноми и карциносаркоми. Саркомите от маточен произход (лейомиосаркоми и ендометриални стромални саркоми) ще следват различна класификация на TNM и FIGO.
FIGO 2009 Поставяне на рак на матката
I етап
Туморът, ограничен до тялото на матката.
AI
Липса на инвазия в миометриума o Онкологичният стадий е един от най-важните прогностични фактори.
- Степен 1: ≤5% неплоскостен или неморулен твърд растеж (добре диференциран).
- Степен 2: 6% до 50% твърд неквамозен или неморулен растеж (умерено диференциран).
- Степен 3: 50% несквамозен или неморулен твърд растеж (слабо диференциран или дедиференциран).
Лечение
Първоначално хирургично лечение на рак на ендометриума:
Хирургията е гръбнакът на лечението. При тези пациенти с ендометриоиден подтип IAG1 рак на ендометриума и без изпълнени генетични желания, те трябва да бъдат оценени в комитет, за да се обмисли отлагането на окончателното хирургично лечение.
Адювантно лечение:
Пригодността на лечението след хирургичния подход се определя въз основа на риска от рецидив. Тези групи са направени въз основа на клиникопатологични прогностични фактори.
Лечение на рецидив:
При пациенти, диагностицирани с локален рецидив (между 25-40%), преди да се предложи каквото и да е лечение, биологията на тумора, интервалът без заболяване, броят на лезиите и местоположението, предишни лечения, резектабилност и общото състояние на пациентите.
При пациенти със системен рецидив лечението ще зависи от хистологията и молекулярната биология. При тези пациенти с нискостепенни ендометриоидни тумори и положителни хормонални рецептори ще се обмисли лечение с хормонална терапия. При висококачествени тумори или неендометриоидни хистологии стандартното лечение ще се състои от карбоплатин и паклитаксел. Наскоро лечението от втора и трета линия имунотерапия показват високи нива на отговор при монотерапия при пациенти с дефицит на възстановителни гени или мутация в POLE или в комбинация (пембролизумаб и ленватинибит), независимо от състоянието на възстановителните гени. Вече се провеждат опити с първа линия имунотерапия, за които все още нямаме резултати. В контекста на метастатичното заболяване, клиничните изпитвания винаги трябва да бъдат възможност за обмисляне.
Терапевтично бъдеще:
За пациентите в начални етапи целта е:
- Проектирайте нови методи за откриване.
- Проектирайте протоколи за управление на контролен възел.
- Проектирайте нови хормонални терапии с намерението да запазите плодовитостта, особено при млади пациенти.
- Намаляване на токсичността, свързана с лъчева терапия.
- Интегриране на молекулярния профил в адювантното лечение, така че, в зависимост от профила, да се оцени пригодността на лъчетерапията в началните етапи и дори да се изясни ползата от химиотерапията при високорискови пациенти.
За пациенти в напреднал стадий:
- Най-изследваните пътища са имунотерапия и PI3K/AKT/mTOR (70% от проучванията срещу молекулярни цели при рак на ендометриума).
- В имунотерапията преобладават инхибиторите на контролните точки. Те са от особен интерес за ултра и хипермутираните групи, тъй като имат по-голямо количество неоантигени, лимфоцитна инфилтрация и експресия на PD1/PDL1.
- Пътят PI3K/AKT/mTOR изглежда е от особен интерес за подтипа с нисък брой копия и подтипа на ендометриоидите. Преобладават комбинациите с хормонална терапия. Вече има някои доказателства в клинични проучвания с темсиролимус, летрозол-еверолимус и темсиролимус-бевацизумаб.
Проследяване
Повечето рецидиви се появяват през първите три години след поставяне на диагнозата. Целта на проследяването се състои от ранно откриване на рецидив на заболяването и допълнително позволява да се контролира въздействието на лечението върху качеството на живот.
Повечето рецидиви са симптоматични, като най-чести са наличието на кръв в урината (хематурия), кръв в изпражненията (ректория/хематохезия) и вагинално кървене; в случай на представяне на пациента трябва да бъде насочен към консултация за оценка.
Прегледите ще бъдат определени в зависимост от риска от рецидив, но като цяло те ще се провеждат на всеки 3-6 месеца през първите две години след края на лечението и впоследствие поне до петата година на всеки 6-12 месеца.
Всеки преглед трябва да включва поредица от въпроси, които могат да ни накарат да подозираме локален рецидив, като например да знаем дали е имало кървене, болка, стомашно-чревни смущения или дизурия. Трябва да попитаме и за краткосрочните и дългосрочните неблагоприятни ефекти от лечението. Трябва да се използва за популяризиране на здравословни навици в офиса. Пълно физическо изследване трябва да се извърши с палпация на ганглиозните вериги и коремен преглед, гинекологичният преглед ще включва най-малко преглед със спекулум, бимануален преглед и биопсия на всяка подозрителна лезия с нов вид. Вагиналната цитология при проследяване на рак на маточната шийка не се препоръчва и дори се счита за неподходяща практика. Определянето на туморния маркер Ca125 по време на проследяване може да се обмисли при тези пациенти с повишена диагноза или серозна хистология, но не е част от обичайното проследяване.
Образните тестове (рентгенография на гръдния кош, компютърна томография или абдоминална ехография) при асимптоматични пациенти откриват между 0-30% от рецидивите, така че те не се препоръчват рутинно. Пригодността за извършване на някои образни тестове при проследяването също трябва да се оценява индивидуално, като например в случаите на FIGO етап III-IV по време на диагнозата, където може да се препоръча компютърна томография гръден кош-корем-таз. Семестър през първия 2-3 години.
Дългосрочни неблагоприятни ефекти от лечението:
- HDL холестеролът, когато качеството е по-важно от количеството - Испанско кардиологично общество
- Растителни антиоксиданти, испанско общество за диета и наука на Паркинсон и Алцхаймер
- Присъствахме на XIV среща по въпросите на затлъстяването, диабета и храненето на Испанското медицинско общество
- Бюлетин на Испанското общество по биология
- Здравословна и устойчива храна, предизвикателството на обществото на 21-ви век - Gaceta Médica