Вижте статиите и съдържанието, публикувани в този носител, както и електронните резюмета на научни списания към момента на публикуване
Бъдете информирани по всяко време благодарение на сигнали и новини
Достъп до ексклузивни промоции за абонаменти, стартиране и акредитирани курсове
The Вестник по медицина и изследвания е научна публикация на Автономния университет на щата Мексико. На всеки шест месеца той приема статии на испански и английски език и разглежда за публикуване онези произведения, свързани с медицински изследвания във всичките му аспекти. Оригинални статии, прегледни статии, научни писма, клинични насоки, консенсус, редакционни коментари, писма до редакторите, статии за историята и изкуството на медицината с академичен характер, които включват резултати от изследвания със съдържание от областите, се приемат за публикуване. кардиология, пулмология, нефрология, гастроентерология, ревматология, гинекология, генетика, фармакология, имунология, молекулярна биология, вътрешни болести, обществено здраве, обща медицина, наред с други.
Вестник по медицина и изследвания е научно списание на Universidad Autónoma del Estado de México. Той публикува два пъти годишно статии на испански и на английски език и ще разгледа за публикуване онези произведения, свързани с медицинското разследване във всичките му аспекти. Списанието приема за публикуване оригинални статии, прегледни статии, научни писма, клинични насоки, консенсус, редакционни коментари, писма до редактори, статии и история на медицината, включително с резултати от академични изследвания със съдържание от областта на кардиологията, пулмологията, нефрология, гастроентерология, ревматология, гинекология, генетика, фармакология, имунология, молекулярна биология, вътрешни болести, обществено здраве, обща медицина, наред с други.
Следвай ни в:
- Въведение
- Патофизиология
- Клинични проявления
- Диагностика и лечение
- Финансиране
- Въведение
- Концептуална идентификация на синдрома на Leigh
- Биохимични основи на синдрома на Leigh
- Патофизиология
- Клинични проявления
- Наследяване на синдрома на Leigh
- Диагностика и лечение
- Финансиране
- Конфликт на интереси
- Благодаря
- Библиография
Изследването на структурата, физиологията и нарушенията, свързани с митохондриите, са били теми на изследване за много учени през цялата история, можем да се позовем на 1951 г., в която Денис Ли описва случая на дете със собствени клинични прояви на синдрома, който днес носи неговото име, за което са известни все повече и повече, но е постигнат малък напредък в създаването на лечение, което успява да увеличи продължителността на живота на страдащите от него.
Човешкото тяло като перфектна машина изисква приноса на биологични горива (въглехидрати, липиди и протеини), необходими за получаване на химическата енергия, необходима от различни биологични процеси и по този начин за поддържане на хомеостазата. Метаболизмът на тези горива в организма се постига чрез използването на различни катаболни и анаболни пътища, които изискват координирано функциониране на клетъчните елементи, тоест добра комуникация между органелите на която и да е клетка в тялото.
След правилния метаболизъм на биогоривата в клетките, най-накрая получаваме химични енергийни молекули под формата на АТФ, които са необходими за осъществяване на процеси като; преминаване на молекули през клетъчната мембрана, движение на бичури, мускулна контракция, наред с много други жизненоважни функции. По-голямата част от тази химическа енергия се получава благодарение на участието на митохондриите, в чиято структура е разположена важната дихателна верига за извършване на окислително фосфорилиране и накрая получаването на АТФ.
Концептуална идентификация на синдрома на Leigh
Невродегенеративно разстройство, вторично вродено отсъствие на: Пируват дехидрогеназен комплекс, Комплекс I, IV или V на дихателната верига 1 .
Биохимични основи на синдрома на Leigh
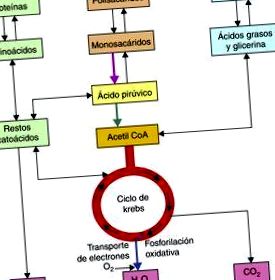
Метаболитните пътища, които се използват както в катаболизма на въглехидратите, липидите и протеините, се сближават в митохондриите след окончателното образуване на молекули ацетил КоА 2, които впоследствие ще се метаболизират от цикъла на трикарбоксилната киселина, за да се получат редуцирани кофактори, NADH + H и FADH2, който след това ще бъде окислен в дихателната верига, за да се получат АТФ молекули (фиг. 1).
Получаване на ацетил CoA.
В случай на въглехидрати, аеробната и анаеробната гликолиза са важни пътища за използването на тези молекули, след поредицата от реакции, които анаеробната гликолиза предполага в клетъчния цитозол, стигаме до получаването на пируват, който ще бъде субстрат за пируватдехидрогеназата. комплекс, който ще окисли молекулата на пирувата до ацетил КоА в митохондриите.
Молекулата на ацетил КоА се формира от коензим А, чиято молекула съдържа аденин, рибоза, пантотенова киселина и тиолова група, последната реагира с карбоксилните групи, така че молекулата на ацетил КоА най-накрая се получава, това е съединение с висока енергия, така че може да дари вашата ацетилова група в цикъла на трикарбоксилната киселина.
В цикъла на трикарбоксилната киселина молекулата на ацетил КоА ще се метаболизира до CO 2 и H 2 O, също така в серията от реакции, които са част от този цикъл; 3 NADH + H, 1 FADH 2 и GTP молекула. Редуцираните кофактори (NADH + H и FADH2), които се произвеждат в този цикъл, са важни, тъй като те действат като транспортери на електроните, получени след катаболизма на биогоривата, следователно тези кофактори, получени от цикъла на Кребс или от трикарбонови киселини, ще впоследствие дарява тези електрони на първия комплекс на дихателната верига в случай на кофактор NADH + H или на комплекс II в случай на кофактор FADH2, след поредица от реакции, при които тези кофактори се окисляват и комплексите се редуцират ( фиг. 2).
Намалените кофактори, получени при анаеробната гликолиза на клетъчния цитозол, не могат да преминат през митохондриалната мембрана, поради което, за да влязат, те използват глицерол - 3 - фосфатните совалки (главно в мозъчните и мускулните клетки) и малат - аспартата (главно в черния дроб и сърце), които въвеждат електроните на редуцираните кофактори от цитоплазмата в митохондриите.
Преминаването на електрони през дихателната верига започва в комплекс I или II, по-късно те преминават към убихинон (Q), след това към комплекс III, това намалява до цитохром и накрая цитохромът намалява до комплекс IV, който ще дари 2 електрона на кислорода за образуването на водна молекула, трябва да се отбележи, че преминаването на електрони през ензимните комплекси на дихателната верига се извършва от комплекса, който има по-нисък стандартен потенциал за редукция до комплекса, който има по-висок стандартен редукционен потенциал, т.е. от комплекса с по-нисък афинитет към електроните до комплекса, който има по-висок афинитет към тях.
Преминаването на електрони през комплексите на дихателната верига е съчетано с изпомпването на протони от комплекси I, III и IV в междумембранното пространство, като по този начин се създава електрохимичен градиент в това пространство, тенденцията на протоните. стабилизира градиента от двете страни на вътрешната митохондриална мембрана, това ще им позволи да преминат през АТРазния комплекс, чиято структура се основава на субединица F 1 и F 0. Субединицата F 0 образува канала, през който преминават протоните, докато субединицата F 1 е мястото, където от ADP и Pi се осъществява образуването на молекулата ATP, следователно е важно да се отбележи, че енергията, която се генерира след протоните преминават през този канал, позволяват на молекулата АТФ, образувана от субстратите (ADP и Pi) да се освободи, не трябва да се мисли, че енергията, получена при преминаването на протоните, е правилно енергията, съдържаща се в АТФ.
След получаване на АТФ молекули, те могат да се използват в широк спектър от физиологични процеси, които го изискват за добро функциониране и поддържане на жизненоважен баланс за човешкото същество.
В тялото има тъкани, които се открояват с изискването за непокътнат оксидативен метаболизъм, който осигурява получаването на необходимата енергия за ефективно изпълнение на функцията си, в тези тъкани преобладава централната нервна система, в рамките на която се открояват базалните ганглии представяйки висока метаболитна активност, ситуация, която ги прави уязвими към увреждане на клетките, така че неуспехите в клетъчния метаболизъм на тези структури ще бъдат значително отразени в контролните функции, които те изпълняват в тялото.
Базалните ганглии (globus pallidus, putamen, опашко ядро, субталамично ядро и substantia nigra) са натрупвания на невронни тела, чиято основна функция е да контролират началото, амплитудата и бързината на движенията. Окислителният метаболизъм и некрозата на тези структури се превръщат в дефекти в движението, следователно те се характеризират с двигателни дефицити или необичайно активиране на двигателната система, което води до скованост, тремор и неволни движения (Фиг. 3).
Базална ганглия некроза.
Намаляването на производството на АТФ, което се случва при този синдром, не се ограничава до неговите въздействия върху централната нервна система, последиците от това намаляване на енергията се отразяват в клиничните прояви на синдрома на Leigh.
Припадъци, психомоторна изостаналост, оптична атрофия, хипотония, слабост, летаргия, повръщане, абнормни движения (атаксия, тремор), раздразнителност, загуба на зрение и дихателни аномалии 3 .
Наследяване на синдрома на Leigh
Въпреки че митохондрията има своя собствена ДНК, тя не е независима от участието на ядрена ДНК, тъй като и двете участват в кодирането на субединиците, изграждащи всеки от ензимните комплекси на дихателната верига, с изключение на комплекс II. изключително кодиран от ядрена ДНК, поради което в зависимост от засегнатия комплекс и неговото кодиране, типът на наследяване може да бъде: майчин, в случай на мутации в митохондриална ДНК или автозомно-рецесивен, когато мутациите възникват в ядрената ДНК 5 .
Най-докладваните случаи на синдром на Leigh са идентифицирани чрез мутации в митохондриална ДНК, чийто ген кодира една от субединиците на ATPase, поради което той представлява наследство от майката, от друга страна, мутации в ядрена ДНК, които засягат синдрома на комплекс IV представя автозомно-рецесивно наследство. Честотата на представяне на този синдром е 1 на 36 000 раждания.
Диагностика и лечение
Клиничните прояви на синдрома се проявяват преди 6-месечна възраст, лекарят, оценяващ случая, изисква големи умения, за да може да разграничи това разстройство от други митохондриални разстройства, които имат подобни характеристики и с които може да се обърка, за диагноза Адекватен диференциал трябва да се използват ресурси като; Мускулна биопсия за анализ на функционирането на дихателната верига и за идентифициране на грешката в ензимните комплекси, както и използването на магнитен резонанс и компютърна томография, която позволява да се идентифицира некрозата на базалните ганглии, основната характеристика на Leigh синдром.
Лечението след диагностицирането на този синдром е палиативно, прилагането на кетогенна диета, когато синдромът е свързан с дефицит на пируват дехидрогеназа, може да не отразява никаква полза, поради липсата на ефективно лечение, което позволява да се намалят щетите, продължителността на живота на детето с този синдром не надвишава 2 години.
Не е получено спонсорство за изпълнението на тази статия.
Конфликт на интереси
Авторът не декларира конфликт на интереси.
На д-р Аурелио Мендоса Меделин, професор в учебния отдел по биохимия към Медицинския факултет на Автономния университет на щата Мексико, за знанията, допринесли за извършването на тази статия.
- С; Синдром на Leigh с d; дефицит на комплекси I; III и IV на митохондриалната дихателна верига
- ЛЕЧЕНИЕ НА ЗАБОЛЯВАНЕТО НА HIRSCHSPRUNG, СРЕДСТВО ПО МЕДИЦИНА
- Списание за холистична медицина Допълнителни лекарства №53
- Автономно списание за лични изследвания
- Диетичен риск; за наличието на дислипидемии при ученици Revista de Medicina e