- Субекти
- Обобщение
- Въведение
- Разпределение на телесните мазнини и риск
- Съхранение и освобождаване на мастни киселини.
- Образуване на адипокини в регионалната мастна тъкан.
- Лептин
- Адипонектин
- Възпалителни цитокини
- Други адипокини
- Загуба на глутеофеморална мастна тъкан и заболявания
- Излишък на глюкокортикоиди
- Липодистрофия
- Завършеност
Субекти
Обобщение
Въведение
Затлъстяването се определя като индекс на телесна маса (ИТМ)> 30 kg m –2, а повишеният ИТМ е свързан с висок риск от сърдечно-съдови заболявания и диабет. 1 Отдавна е известно, че разпределението на телесните мазнини също е важен рисков фактор: съотношението на коремната мастна тъкан към глутеофеморалната телесна мазнина, измерено например чрез съотношението между талията и ханша, е свързано със свързаните със затлъстяването заболявания и смъртност и по-силен маркер за сърдечно-съдови рискове от ИТМ. 2, 3, 4 Тук разглеждаме доказателствата, че глутеофеморалната мазнина е защитна и възможните механизми, които могат да бъдат включени.
Разпределение на телесните мазнини и риск
Няколко популационни проучвания подкрепят факта, че рисковете за здравето, свързани със затлъстяването, зависят от натрупването на коремни мазнини. Коремното затлъстяване е свързано с повишено кръвно налягане и нива на триглицериди в плазмата (TG). 2, 3 Също така е независим предиктор за развитието на диабет тип 2. 5 5
Неблагоприятният ефект на коремното затлъстяване възниква от комбинацията от дисфункция на подкожната мастна тъкан и натрупването на висцерална мастна тъкан, което става очевидно, когато индивидите с повишено съотношение талия-ханш се изследват с образни техники. 6, 7, 8 Особеното значение на натрупването на висцерална мазнина спрямо дисфункцията на съхранението на подкожната мазнина наскоро беше поставено под въпрос 9, 10, тъй като има все повече доказателства в подкрепа на това, че висцералните адипоцити са фенотипно различни от подкожните адипоцити. единадесет
Таблица в пълен размер
Защитният ефект на глутеофеморалната мазнина също е потвърден в големи проучвания с популация. В проучването AusDiab, по-голямата обиколка на тазобедрената става е свързана с по-ниско разпространение на недиагностициран захарен диабет и дислипидемия. 27 Проучването INTERHEART, състоящо се от 27 000 участници, установява независима връзка между по-голямата обиколка на тазобедрената става и по-ниския риск от инфаркт на миокарда. 4 В Европейското проспективно изследване на рака и храненето - проспективно проучване на Норфолк, по-голямата обиколка на тазобедрената става е свързана с по-ниско съотношение на риск от коронарна болест на сърцето. 28 Освен това обиколката на тазобедрената става е положително свързана с плазмените нива на аскорбинова киселина, антиоксидантен фактор, за който се смята, че допринася за ендотелната защита. 29
Последните физиологични и молекулярни проучвания, които изясняват възможните механизми, които могат да допринесат за защитната роля на глутеофеморалното депо, ще бъдат фокусът на този преглед. Предполага се, че подкожната мастна тъкан действа като буфер за ежедневния прием на липиди в диетата, предпазвайки други тъкани от липидно преливане със свързана липотоксичност. 30 Защитните свойства на глутеофеморалната мазнина могат да бъдат получени от диференциално локално управление на абсорбцията и освобождаването на мастни киселини. Всъщност натрупването на феморална мастна тъкан, което е типично за женския модел на разпределение на мазнините, е свързано с повишена активност на липопротеиновата липаза в мастната тъкан. 31,32 Предвид метаболитната и сърдечно-съдовата защита, предавани от модела на разпределение на гиноидната мазнина, това подкрепя идеята, че глутеофеморалната мазнина е защитна "метаболитна мивка". 33
Друга възможност е, че има диференциална секреция на протеини, свързани с мастната тъкан, т.е. адипокини. Както ще бъде обсъдено по-късно, глутеофеморалната мастна тъкан може да допринесе за защитен адипокинов профил, като секретира повече „полезни“ адипокини и по-малко провъзпалителни молекули в сравнение с коремните мазнини.
И накрая, състояния, които водят до загуба на глутеофеморална мазнина, като хроничен излишък на глюкокортикоиди при синдрома на Кушинг (CS) или частична липодистрофия, водят до метаболитни аномалии, които подчертават защитните свойства на този отличителен депозит на мастна тъкан.
Съхранение и освобождаване на мастни киселини.
Метаболизмът на мастната тъкан е сложен и силно регулиран процес, който зависи от няколко фактора. 34 Една от основните функции на подкожната мастна тъкан е краткосрочното и дългосрочно съхранение на енергия като TG за попълване на тялото с енергия под формата на неестерифицирани мастни киселини, отделяни по време на тренировки, гладуване или гладуване. . Важни определящи фактори за местния трафик на мастни киселини от мастната тъкан са скоростта на липолиза, скоростта на съхранение на TG, която се случва главно след хранене, и притока на кръв в тъканните легла. 35 Вариациите на тези фактори може да са отговорни за благоприятните ефекти на глутеофеморалните мастни запаси.
Инсулинът е основен подтискач на липолизата в мастната тъкан. Разпределението на телесните мазнини влияе върху инхибирането на липолизата: адипоцитите, изолирани от затлъстели жени в горната част на тялото, са по-малко чувствителни към инсулина в сравнение с тези при затлъстелите жени в долната част на тялото. 36 Катехоламините увеличават липолизата в изолирани адипоцити. Съществуват обаче значителни разлики между депозитите по отношение на този отговор. Коремните адипоцити показват четири до петкратно увеличение на липолизата по време на стимулация с норепинефрин в сравнение с глутеалните адипоцити. 37 Това се медиира от повишена експресия на бета-адренорецептори в коремното депо. 38
Абсорбцията на мастни киселини от богати на TG хиломикрони от храна зависи от експресията на липопротеинова липаза (LPL) от адипоцитите. В изолирани адипоцити и мастни сегменти експресията на LPL иРНК е по-висока в коремните клетки, отколкото в глутеалните клетки. 39 Ситуацията обаче е може би по-сложна, главно поради сложната посттранскрипционна регулация на LPL. 40 Това се наблюдава при анализ на сексуалния диморфизъм на разпределението на мазнините: активността на LPL е по-висока в коремните адипоцити на мъжете и в глутеалните адипоцити на жените, съответно в другия депозит. 31, 39 При мъжете тестостеронът потиска активността на LPL в бедрото, което допринася за натрупването на коремни мазнини. 41 Следователно е вероятно образуването на специфични за пола мастни натрупвания да се регулира частично от LPL.
В резултат на сложността на метаболизма на човешката мастна тъкан, изследването на мастните натрупвания in vivo е единственият начин, който позволява интегрирането на фактори, които не присъстват in vitro. Горната част на телесните мазнини допринася основно за неестерифицираните системни мастни киселини, следователно тя показва по-висока степен на липолиза в сравнение с по-ниска телесна мазнина. 42, 43 Скоростта на действие на хормон-чувствителния липазен ензим, ключов ензим в липолизата, е по-ниска в глутеуса, отколкото в коремния резервоар. 44 Гладуването за 72 часа води до повишена липолиза в коремното депо, но не и в глутеофеморалната мастна тъкан. 45 По време на стимулация на епинефрин, коремната липолиза изглежда по-висока от липолизата на бедрената кост, когато се измерва като освобождаване на глицерол чрез микродиализа. 46 Освобождаването на палмитат, директен маркер за липолиза, е по-ниско в мазнините в краката в сравнение с отлагането в корема по време на системна бета-адренорецепторна стимулация. 47
Регионални разлики могат да бъдат открити и при изучаване на абсорбцията на мастни киселини in vivo. Последователна констатация, много в съответствие с по-ниските нива на липолиза в глутеофеморалните телесни мазнини, е, че коремните мазнини абсорбират мастни киселини, получени от ястия, с по-голяма чувствителност от по-ниските телесни мазнини всеки ден. 48,49 Това подкрепя хипотезата, че подкожните мазнини са метаболитна „мивка“, като по-голямата част от ежедневното буфериране на мастни киселини се обработва от коремните мазнини. Точният трафик на мастни киселини обаче може да бъде по-сложен, предвид наличието на предполагаеми различни пътища за оборота на липопротеини с много ниска плътност и оборота на неестерифицирани мастни киселини, например. Те, както и регулирането на дългосрочното отлагане на мастни киселини в запасите на мазнини в долната част на тялото, са слабо разбрани и изискват допълнително проучване.
Кръвният поток на мастната тъкан (ATBF) е важен фактор, определящ метаболизма на мазнините, който може да бъде изследван само in vivo. Вариациите в кръвния поток позволяват регулиране на освобождаването на нестерифицирани мастни киселини в системната циркулация и наличието на субстрат за LPL след хранене. За разлика от това, ATBF се увеличава в периоди на глад и след хранене. 50, 51 Интересното е, че повишаването на ATBF след хранене не е директен ефект на инсулина, а основно се медиира от катехоламини и азотен оксид. 52, 53
ATBF промените в съхранението на мазнини в корема са добре проучени в различни условия; малко обаче се знае за регулирането на ATBF в мастното депо на долната част на тялото. Доказано е, че глутеалната мазнина има по-нисък изходен ATBF, 44, а при слабите жени ATBF на бедрената кост показва намалено увеличение по време на системна стимулация на епинефрин в сравнение с коремните мазнини. 46 Постпрандиално ATBF се увеличава както в коремните, така и в бедрените отлагания при жените, но само в коремните запаси при мъжете. 49 Ще са необходими още проучвания, за да се изяснят точните механизми зад диференциалната регулация на ATBF на двата резервоара.
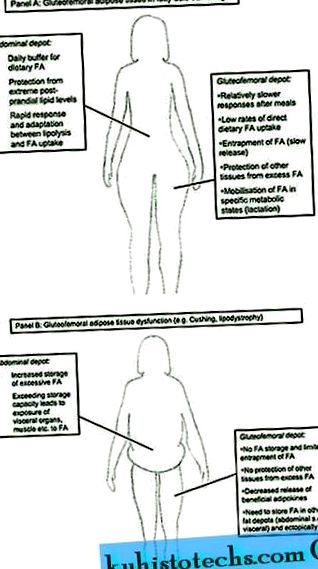
Роля на глутеофеморалната мастна тъкан в ежедневния метаболизъм ( да се ); дисфункция на глутеофеморалната тъкан и метаболитно здраве ( б ). Съкращения: FA, мастна (и) киселина (и); sc, подкожно.
Изображение в пълен размер
Образуване на адипокини в регионалната мастна тъкан.
Известно е, че мастната тъкан отделя няколко хормона, наречени адипокини. Терминът „адипокини“ представлява общия източник на тези хормони 57, но не взема предвид, че те всъщност се секретират от различни видове клетки в тъканите. Следователно, докато адипокини като адипонектин и лептин се произвеждат от адипоцити, интерлевкините се секретират главно от резидентни макрофаги. Откъдето и да идват, адипокините са част от сигнална каскада, която се разбира само частично, позволявайки комуникация между мастната тъкан и други органи, предимно мозъка и черния дроб. Съществуването на такава комуникационна мрежа не е изненадващо, като се има предвид централната роля на тъканта за съхранение и освобождаване на мазнини и необходимостта от координация и контрол на апетита, глада и ситостта, които са обект на централна регулация. Въпросът, който възниква, е дали защитните свойства на долните телесни мазнини са свързани с полезен профил в метаболизма на адипокините.
Разликите в експресията и секрецията на ген на адипокин in vitro са добре установени при сравняване на подкожната и висцералната мастна тъкан. 11, 58 Въпреки това, малко се знае за разликите между мазнините в горната и долната част на тялото.
Лептин
Адипонектин
Възпалителни цитокини
Заедно с "класическите" адипокини лептин и адипонектин, няколко от така наречените възпалителни цитокини са идентифицирани като секретирани от мастната тъкан. Това се признава като една от връзките между затлъстяването и развитието на сърдечно-съдови заболявания, инсулинова резистентност и диабет, тъй като възпалителните процеси са част от патофизиологията на тези заболявания. Най-широко анализираните цитокини са тумор некрозис фактор алфа (TNF-α) и интерлевкин 6 (IL-6).
IL-6 е възпалителен цитокин, който подобно на TNF-α се секретира от различни клетки и тъкани, 116 включително мастна тъкан. Там той се секретира както от адипоцитите, така и от клетките на стромаваскуларната фракция и нивата на секреция са в положителна корелация със затлъстяването. 117, 118 Системните плазмени нива на IL-6 корелират с висцералната мастна маса и има слаба отрицателна връзка с увеличената площ на мазнините в бедрото. 119 Няма проучвания, сравняващи регионалното производство на IL-6 между мазнини в горната и долната част на тялото, но директното in vivo регионално измерване на концентрациите на IL-6 и IL-6 рецепторите показва, че коремната тъкан освобождава IL-6, но не и вашия приемник. 111, 112 Въпреки че инсулиновата резистентност и сърдечно-съдовите заболявания се считат за хронични възпалителни процеси в частично ниска степен, ролята на IL-6 в развитието на инсулинова резистентност остава противоречива. Понастоящем липсват данни за регионалното освобождаване на IL-6 и това е област на бъдещи изследвания.
Други адипокини
В момента има няколко други известни адипокини и някои от тях показват интересни взаимовръзки между системните нива и параметрите на разпределение на телесните мазнини. Например плазмените нива на ретинол-свързващ протеин 4, протеин, освободен от адипоцитите и свързан с инсулинова резистентност, 121 корелират с мастната маса на багажника. 122, 123 В допълнение, серумният васпин, сенсибилизиращ инсулина адипокин, показва интересен сексуален диморфизъм с по-високи нива при жените. 124 За тези и други възникващи адипокини малко се знае за специфичната роля на регионалната мастна тъкан в нейното производство, секреция и функция в метаболизма на човека.
Загуба на глутеофеморална мастна тъкан и заболявания
Досега бяха подчертани полезните свойства на глутеофеморалната мастна депа. Друга перспектива, която подчертава неговите защитни характеристики, е да се изясни какво се случва, когато се загубят значителни количества глутеофеморална мастна маса. Всъщност загубата на мазнини в долната част на тялото е свързана с метаболитни нарушения.
Излишък на глюкокортикоиди
Липодистрофия
Вредният ефект на загубата на глутеофеморална мазнина е най-очевиден при липодистрофичните синдроми. Липодистрофията се характеризира с частично или пълно отсъствие на мастна тъкан и може да бъде наследена или придобита. 134 Загубата на мастна тъкан води до натрупване на извънматочна мазнина, в съответствие с идеята, че подкожната мастна тъкан е „метаболитна мивка“ за излишната енергия. 33, 135 Натрупването на извънматочна мазнина се случва в черния дроб, панкреаса и мускулите. Също така, в зависимост от вида липодистрофия, има натрупване на мазнини в специфични неатрофични мастни натрупвания, например шията.
Пациентите с автозомно-доминантна фамилна частична липодистрофия тип Dunnigan губят главно подкожната мастна тъкан в ръцете и краката си. 135 Тези пациенти показват тежка инсулинова резистентност, аномалии на липидния профил, хипертония и развиват диабет. 136, 137, 138 Няколко мутации в гена LMNA и в гена PPARG са идентифицирани като молекулен механизъм, отговорен за развитието на фамилна частична липодистрофия. 134 PPARG мутации осигуряват възможна връзка между дисфункцията на мастната тъкан и метаболитния профил, свързан с този тип липодистрофия, тъй като изглежда, че мастната тъкан не реагира на физиологичните регулаторни механизми при тези пациенти. 138
За разлика от това, пациентите с придобита частична липодистрофия (синдром на Barraquer-Simons), които постепенно губят мастната си тъкан от лицето и горната част на тялото, но депонират големи количества мазнини в глутеофеморалната област, показват лека инсулинова резистентност и имат по-ниска честота на диабет в сравнение с други липодистрофични синдроми. 134, 139
Завършеност
- Телесните мазнини могат да представляват по-голям риск за здравето от тама; или тяло
- Мазнини, комбинирани със захар, еликсир за телесни мазнини; Здраве; MASmusculo блог
- Канелата може да ви помогне да отслабнете и да лекувате диабет Salud La Revista El Universo
- Патладжанът ви помага да намалите коремните мазнини - По-добре със здравето
- Кърменето като защитен фактор срещу рак на гърдата: библиографски преглед - сп