Испанската асоциация по педиатрия има за една от основните си цели разпространението на строга и актуална научна информация за различните области на педиатрията. Anales de Pediatría е органът за научно изразяване на асоциацията и представлява превозното средство, чрез което сътрудниците комуникират. Той публикува оригинални трудове за клинични изследвания в педиатрията от Испания и страни от Латинска Америка, както и преглед на статии, изготвени от най-добрите специалисти във всяка специалност, годишните съобщения на конгреса и протоколите на Асоциацията, както и ръководства за действие, изготвени от различните общества/Специализирани Секции, интегрирани в Испанската асоциация по педиатрия. Списанието, еталон за испаноезичната педиатрия, е индексирано в най-важните международни бази данни: Index Medicus/Medline, EMBASE/Excerpta Medica и Index Médico Español.
Индексирано в:
Index Medicus/Medline IBECS, IME, SCOPUS, Разширен индекс за научно цитиране, Доклад за цитиране на списания, Embase/Excerpta, Medica
Следвай ни в:
Импакт факторът измерва средния брой цитати, получени за една година за произведения, публикувани в публикацията през предходните две години.
CiteScore измерва средния брой цитати, получени за публикувана статия. Прочетете още
SJR е престижна метрика, базирана на идеята, че всички цитати не са равни. SJR използва алгоритъм, подобен на ранга на страницата на Google; е количествена и качествена мярка за въздействието на дадена публикация.
SNIP дава възможност за сравнение на въздействието на списанията от различни предметни области, коригирайки разликите в вероятността да бъдат цитирани, които съществуват между списанията на различни теми.
За първи път описан през 1964 г. 1, синдромът на Швахман-Даймънд (SSD) е рядко автозомно-рецесивно заболяване, с приблизителна честота 1 на 100 000 раждания 2,3 и съотношение мъже: жени 1,7: 1 3, 4. Това е втората причина за вродена екзокринна панкреатична недостатъчност в детска възраст след муковисцидоза.
SSD е мултисистемно заболяване, характеризиращо се с екзокринна панкреатична недостатъчност, дисфункция на костния мозък, промени в скелета и нисък ръст 2,5-8. Прогнозата на пациентите се определя от повтарящите се бактериални инфекции, вторични главно поради промяната на неутрофилите, както и от гръбначната дисфункция и левкемията.
Генът SBDS наскоро беше идентифициран като ген, отговорен за SSD. Този ген е разположен на нивото на хромозома 7, в локуса 7q11 5,9,10 .
В тази статия ще опишем клиничния случай на бебе, което е диагностицирано с този синдром в нашата услуга.
14-месечно бебе е насочено към нашата служба за изследване на хипертрансаминаземия и стагнация на теглото от 9-месечна възраст.
Детето не е представило съответна семейна или лична история. Теглото при раждане е 3390 g, а височината 51 cm. Той е представил адекватно законоустановено развитие на теглото до 9-месечна възраст, като в този момент той започва да има 4-5 лепкави изпражнения с миризма на гранясване на ден заедно със законоустановена стагнация.
В резултат на състоянието педиатърът му направи анализ, при който се открояват само GOT от 464 U/l и GPT от 514 U/l. Той също имаше някои маркери на цьолиакия, които бяха нормални.
Три месеца по-късно, поради постоянството на хипертрансаминаземия, той беше насочен към нашата служба за проучване.
Физикалният преглед разкрива хармоничен микрозомален външен вид, с тегло и височина под 3-тия процентил.Останалата част от изследването беше нормална.
Допълнителните проведени тестове бяха следните:
Хемограма: 8 400 левкоцити (N, 16%; L, 77%; M, 5,8%), хематокрит 34,6%, хемоглобин 11,6 g/dl и 313 000 тромбоцити.
Обща биохимия: GOT, 417 U/l; GPT, 440 U/L; нормален билирубин, GGT и алкална фосфатаза.
Тест за нормална пот.
Ван де Камер: няма стеаторея. Еластаза на изпражненията 11,5 μg/g.
Вирусни хепатитни серологии, 1-антитрипсин, нормален метаболизъм на мед и цинк.
Абдоминален ултразвук: силно изразена свръхплътност на панкреаса, предполагаща екзокринна панкреатична недостатъчност.
В обобщение установихме картина на екзокринна панкреатична недостатъчност, диагностицирана от практически неоткриваема еластаза в изпражненията и съвместимо ултразвуково изследване, с нормален тест за пот, повторен два пъти. Освен това детето е имало забавяне на растежа и лека неутропения. Със съмнението за SSD продължихме да провеждаме нормално рентгенологично костно изследване и генетично изследване, което установи, че детето е хетерозиготно, съставено от две мутации в гена SBDS (258 + 2T> C/183-184TA> КТ), с която поставяме диагнозата SSD при детето.
Същото генетично проучване беше проведено при родителите, в резултат на което бащата носи мутация 183-184 TA> CT и майката носи мутация 258 + 2T> C.
Като се има предвид диагнозата, започна лечение с панкреатични ензими и мастноразтворими витамини, подобрявайки външния вид на изпражненията, но не и развитието на теглото, поддържайки теглото и височината под 3-ия процентил.
Броят на неутрофилите варира, достигайки цифри от 540 неутрофила.
Клиничният фенотип на SSD е много разнороден и показва голямо разнообразие от клинични прояви. Основните характеристики на синдрома са екзокринна панкреатична недостатъчност и дисфункция на гръбначния мозък, и двете от съществено значение за поставяне на диагнозата 2,11. По същия начин, забавяне на растежа и промени в скелета са характерни 2,11,12 .
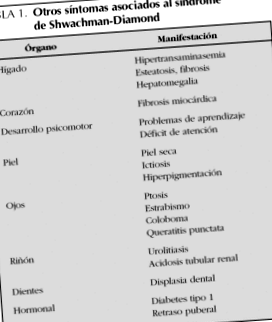
Други възможни находки при SSD са изброени в таблица 1. Кожните, очните и бъбречните промени са много редки.
Първите симптоми и признаци на SSD обикновено се появяват през първата година от живота, какъвто е случаят с нашия пациент 3 .
Когато диагнозата се постави в детска възраст, дисфункцията на панкреаса е налице практически във всички случаи. Типични са ниски концентрации на амилаза (50-75% от пациентите), ниски серумни трипсиногени (70-98%) и променен тест за стимулиране на панкреаса (100%) 2,4. Понастоящем определянето на фекална еластаза е най-ефективният тест за оценка на панкреатична недостатъчност, поради нейната висока специфичност и чувствителност и тъй като нейните стойности не се променят чрез приемане на панкреатични ензими. Тежката панкреатична недостатъчност се счита за ниво на еластаза в изпражненията под 100 μg/g изпражнения 3. По отношение на образни изследвания, ултразвукът на корема показва панкреас с нормален или намален размер, с повишена ехогенност. CT разкрива панкреатична липоматоза 14. В нашия случай диагнозата беше поставена с еластаза на изпражненията от 11,5 μg/g, заедно с предполагаем ултразвук.
Засягането на панкреаса обикновено се подобрява с възрастта в 40-60% от случаите, очевидно поради увеличаване на секрецията на липаза с 2,8 години .
Най-честата хематологична находка е интермитентна неутропения, която се появява в 85-100% от случаите 2,15,16. Независимо от общия брой неутрофили, има и промяна в тяхната миграция, поради което съществува повишен риск от сериозни бактериални инфекции дори при нормален брой неутрофили 11,17. Появата на инфекции определя прогнозата в детска възраст 18. Нашето дете представи фигури до 500 неутрофила в своята еволюция, които се възстановиха спонтанно.
Други хематологични промени, които могат да бъдат открити, са анемия (50-80%), повишени концентрации на фетален хемоглобин (80%) и тромбоцитопения (25-85%) 15,19 .
Забавянето на растежа се появява при 60% от децата и е независимо от храносмилателната малабсорбция, тъй като не се подобрява при добавяне на ензими на панкреаса, нито при нормализиране на функцията на панкреаса, което може да се появи с възрастта. Височина и тегло под 3 8,15 процентила са типични. Изглежда, че забавянето се дължи на присъщ проблем с растежа 2. Нашият случай не е показал подобрение във височината към момента, въпреки добавянето на панкреатични ензими и се наблюдава в консултацията по ендокринология, за да се следи развитието на височината.
Костни изменения могат да се появят при 50-75% от пациентите, въпреки че скорошна статия, която разглежда рентгенологичните промени при 15 пациенти, открива промени при практически всички пациенти 12. Най-честите находки са къси ребра с костохондрално удебеляване, стесняване на гръдния кош, по-очевидно при деца под 2-годишна възраст и метафизарна хондродисплазия на дълги кости (особено в бедрата и коленете), 11 по-очевидни при деца над 6 години години. Други находки са: забавено появяване на центрове за вторична осификация, генерализирана остеопения, анормална тубулация на дългите кости, особено на пищяла и първата метакарпална, клинодактилия, синдактилия и валгусни деформации на коленете и бедрата. При нашето дете не се появиха промени в костната серия, която беше извършена, което може да се дължи на факта, че детето е било много малко по време на извършването му.
Други възможни находки са повишени трансаминази и хепатомегалия, които обикновено присъстват в първите години от живота и обикновено се подобряват без усложнения с възрастта. В нашия случай хипертрансаминаземията беше причината за насочване към нашата консултация.
Последните проучвания показват, че мутациите в гена SDBS присъстват при повечето пациенти с SSD 9,20. Този ген е локализиран в хромозома 7, в локуса 7q11. Двете най-често идентифицирани мутации в медицинската литература в гена SBDS (183-184 TA x CT [K62X] и IVS2 (258) + 2T x C [C84fs], съвпадат с тези, представени от нашето дете 5,21,22. Всеки от родителите е носител на една от двете описани мутации.
Що се отнася до лечението, интервенциите ще се извършват по следния начин:
1. Добавяне на панкреатични ензими и мастноразтворими витамини.
2. Профилактика и лечение на инвазивни инфекциозни заболявания с ранно лечение на фебрилни заболявания.
3. Корекция на хематологични отклонения, когато е възможно.
4. Проследяване и лечение на ортопедични деформации.
Тежката неутропения или рецидивиращи инфекции могат да бъдат лекувани с гранулоцитен колония стимулиращ фактор (G-CSF) 16. Съществуват обаче противоречия относно възможността за ускоряване на развитието на миелопролиферативни синдроми 2,11 .
Може да са необходими трансфузии при пациенти с анемия или симптоматична тромбоцитопения. Еритропоетинът също може да бъде полезен при лечение на анемия.
Хормонът на растежа е изпробван без добри дългосрочни резултати 23 .
Трансплантацията на костен мозък е единственият лечебен вариант за тежка дисфункция на гръбначния мозък и се препоръчва при пациенти с тежка панцитопения и лимфопролиферативни и миелопролиферативни синдроми 11,24-26 .
Прогнозата на това заболяване се определя от инфекции 27 и от появата на хематологични неопластични процеси. Най-честите трансформации са остра миелоидна, остра лимфоидна и младежка хронична миелоидна левкемия 2,3,7. Този риск от злокачествено заболяване се оценява на около 25% 3,4. Рискът е по-висок при деца с прогресивна панцитопения. Средната преживяемост на тези пациенти се оценява на около 35 години 28 .
- Уртикария от fr; или и целиакия при педиатричен пациент; trico Annals of Pediatrics
- С; синдром на микродупликация; n 3q29 Педиатрични анали
- Хранителни препоръки за детето; или педиатрични анали на спортисти
- Бъбречни тумори в ni; по-малко от една година; o Педатрични летописи
- Лечение на бактериален менингит Анали на педиатрията