Субекти
Обобщение
Въведение
Резултати
Gas2/HSP90/HSP40 образува свързан с каспаза-3 протеинов комплекс в оризови суспензионни клетки при топлинен стрес
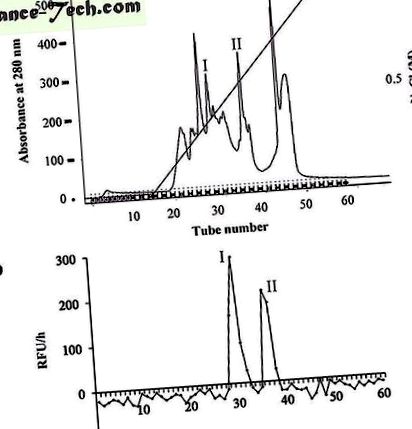
( да се ) Активните фракции на каспаза-3 от колона G-75 се събират и пречистват допълнително на Mono-Q колона, уравновесена с 20 mM Tris/HCl буфер, рН 8.0. Протеините се елуират с NaCl градиент (0
1 М) в 20 mM Tris/HCl буфер, рН 8.0, при скорост на потока от 1 ml/min. Протеините се откриват чрез абсорбция при 280 nm. Събирани са съответно върхове. ( б ) Равен брой пикове, събрани от колоната Mono-Q, бяха инкубирани с Ac-DEVD-AMC. AMC флуоресценцията беше измерена с четец на микроплаки при 30 ° С. RFU/hr представлява относителните разлики във флуоресцентната единица, получени за 1 час. I и II представляват върховете, които проявяват активност, подобна на каспаза-3.
Изображение в пълен размер
Таблица в пълен размер
Профил на експресия на газ2 при различни напрежения.
При физиологични условия Gas2 е некаталитична субединица на глюкозидаза II, която участва в гликозилирането на протеини в ER. За да се идентифицират биологичните функции на Gas2 при абиотичен стрес, експресията на Gas2 се измерва чрез количествена полимеразна верижна реакция в реално време при различни условия, включително при DTT-индуциран ER стрес. Третирането с 6,4 mM DTT индуцира експресията на Os bZIP50 34, маркерният ген за UPR, което показва, че DTT е способен да индуцира ER стрес в клетки в оризова суспензия (фиг. 2а) и при тези условия Gas2 е регулиран надолу ( Фиг. 2б). В допълнение към ER стрес, Gas2 също се регулира надолу при различни абиотични стресове, като студен стрес (фиг. 2в), осмотичен (фиг. 2г) и сол (фиг. 2д).
( да се ) DTT индуцира експресията на OsbZIP50 в клетъчни линии от див тип и OsGas2 RNAi. Протопластите се приготвят от суспензионни клетки и се третират с 6,4 mM DTT в продължение на 18 часа при 26-28 ° С ( б ) Експресия на OsGAS2 в суспензионни клетъчни протопласти с 6.4 mM DTT обработка за различно време. ( в - д ) Експресия на OsGAS2 в корени на 8-дневни разсад с третиране на 4 ° C ( ° С ), 150 mM NaCl ( д ) и 40% от PEG 6000 ( и ) за различно време. Общата РНК беше изолирана за RT-PCR и експериментите бяха повторени три пъти.
Изображение в пълен размер
Клетъчно местоположение
Тъй като Gas2 образува свързан с каспаза-3 протеинов комплекс с GRP94 и HSP40, съдържащ TPR, беше изследвана субклетъчната локализация на тези три протеина. Както се очакваше, Gas2 и GRP94 бяха разположени в ER (фиг. 3а, b), докато HSP40, съдържащ TPR, беше разположен в цитоплазмата (фиг. 3в). Тъй като активността, подобна на каспаза-3, присъства в цитоплазмата, това предполага, че при специфични условия на стрес, съдържащият TPR HSP40 може да образува комплекс с Gas2 и GRP94 на интерфейса ER-цитоплазма, тъй като е известно, че ER осигурява свързващи места за много цитозолни протеини.
Конструкции, носещи 35S: Grp94-GFP, 35S: GAS2-GFP и 35S: GFA2-GFP, бяха съответно въведени в протопласти от стъблата на оризови разсад чрез трансформация, медиирана от PEG-калций. GFP флуоресценция се наблюдава след 16 часа инкубация с конфокален микроскоп PerkinElmer UltraVIEW VoX. Като контрол за локализация на ER се използва ER-Tracker ™ синьо-бял DPX (E12353). Експериментите се повтарят поне пет пъти. Лента = 5 μm.
Изображение в пълен размер
Намаляване на индуцираната от Gas2 автофагия в клетки от суспензия на ориз
Изображение в пълен размер
Gas2 е нов субстрат за каспаза-3-подобна активност в ориза.
( да се ) Неговият таг 6 се слива в N-края на OsGAS2 и мутант D110A/D113A и слетият протеин се експресира в Е. coli. Пречистените диви видове и неговите 6-маркирани мутантни протеини бяха инкубирани съответно с реакционен буфер, каспаза-3 и цитозолна фракция на термично обработени оризови суспензионни клетки. След инкубация, реакционните продукти се анализират чрез 12,5% SDS-PAGE, последвано от имуноблотинг с анти-поли хистидиново антитяло, което разпознава неговия 6-маркиран OsGAS2 N-краен епитоп. Стрелките показват целевите протеинови ленти. ( б ) Схема за фрагментиране на OsGas2 от каспаза-3. OSGas2 с пълна дължина с MW от 74 KDa е илюстриран като линейна молекула с предполагаемо място на разцепване на каспаза-3 DEYD 113, което е обозначено със стрелка. При разграждането на каспаза-3 се получава N-краен фрагмент с MW от 14 KDa (N) и C-краен фрагмент с MW от 60 KDa ( ° С ).
Изображение в пълен размер
Продукт на разцепване на газ-усилена каспаза-3-подобна активност в оризови протопласти
За да се идентифицира възможната функция на продуктите на разпадане на Gas2, фрагменти на Gas2 N и C се експресират в протопласти от оризов мезофил, като се използва индуциран от Dex векторен условен израз и Dex ефективно индуцира експресия на фрагменти (фиг. 6а). В сравнение с експресията на фрагмент N и контрола на вектора, експресията на фрагмент C води до значително увеличение на активността, подобна на каспаза-3 след термична обработка (Фиг. 6Ь). Интересното е, че автофагозомите не са открити в протопласти, експресиращи двата фрагмента след лечение с DTT (данните не са показани).
( да се ) RT-PCR анализ на експресиите на N-крайния фрагмент (N) и С-крайния фрагмент (C) в мезофилни протопласти. Общата РНК се приготвя от протопласти със или без третиране с Dex (контрол) в продължение на 18 часа. 17S РНК се използва като контрола на натоварването. ( б ) Каспаза-3-подобна активност в мезофилни протопласти под експресията на N-крайния фрагмент (N) и С-крайния фрагмент (C). Експресията на N и C се индуцира от Dex в продължение на 18 часа и след това протопластите се третират при 48 ° С в продължение на 15 минути и се оставят да се възстановят при 28 ° С в продължение на 6 часа. Като контрола беше използван протопластът с празния векторен условен израз. Равно количество цитозолни фракции бяха инкубирани с Ac-DEVD-AMC и флуоресценцията на AMC беше измерена за 60 минути с микропроцесор при 30 ° C. RFU/mg: относителни флуоресцентни единици на mg протеин.
Изображение в пълен размер
Дискусия
⊥: път на инхибиране, който е демонстриран в този документ; плътна стрелка: път за активиране, преместване или деградация, който е демонстриран в този документ; стрелка на дъската: пътят, който не е проучен в този документ; кръгов кръг: предполагаемият каспаза-3-подобен ензим. Вижте текста за подробности.
Изображение в пълен размер
Методи
Растителни материали и обработки.
Oryza sativa L. cv. Разсадът Nipponbare се отглежда в течна среда MS при 25 ° C, използвайки 16 h светъл/8 h тъмен цикъл. За лечение на стрес, 8-дневните разсад се инкубират при 4 ° С в плаки или в MS течна среда, съдържаща 150 mM NaCl или 40% PEG-6000 за различни периоди от време. За индуциран от DTT ER стрес, протопластите от 32 клетъчни суспензии бяха инкубирани с течна MS среда, съдържаща 6.4 mM DTT в продължение на 18 часа при 26-28 ° C и след това измити с MS среда два пъти. Равен обем вода се добавя към средата без DTT като отрицателна контрола 41 .
Пречистване и идентифициране на протеини, свързани с активността от типа каспаза-3
Подготовка на протопласт
Клетките от оризова суспензия от GAS2 и линии от див тип RNAi се размножават и култивират при 28 ° С. Протопластите са изолирани от 3 до 4 клетки в суспензия съгласно Maas et al. 42. За изолиране на протопласти от зелена тъкан, оризовите разсад се отглеждат в хранителен разтвор при 28 ° С в продължение на 7-10 дни. 10 cm високи разсад са използвани за изолиране на протопласти според Wang et al. 43 .
Извличане на РНК от разсад от ориз
Общата РНК се изолира от оризови протопласти или корени на разсад, като се използва реактив Trizol (Takara, Япония). Обща РНК (5 μg) е използвана за синтез на cDNA с реактивния комплект PrimeScript ™ RT с gDNA Eraser (Takara, Япония), съгласно инструкциите на производителя.
Количествен анализ в реално време на верижна реакция на полимеразна обратна транскрипция
Количествената полимеразна верижна реакция в реално време се извършва с помощта на CFX 96 флуоресцентен количествен PCR апарат (Bio-Rad, Hercules, CA, USA). Използвани са генно-специфични праймери за откриване на транскрипти на OsGAS2 и 17S rRNA е използвана като вътрешен контрол. Всяка проба беше проведена в три независими експеримента и последователностите на праймерите са подробно описани по-долу.
OsGAS2 -F: TTGGTAAGGAGAAGGAGTTC; OsGAS2 -R: AGGCTGGTGGTACTATGT.
17sRNA -F: ACACGGGGAAACTTACCAGGTC; 17sRNA -R: CCAGAACATCTAAGGGCATCAC.
Изграждане на RNAi-OsGAS2 клетъчна линия.
За да се получи RNAi-OsGAS2, праймерите Ri 1-F/Ri 1-R са проектирани за фрагмент 1 от OsGAS2 и праймери Ri 2-F/Ri 2-R за фрагмент 2 от OsGAS2 (места Kpn I/Sac I и Mlu I/Сайтовете на BamH I са показани в курсив):
Ri 1-F: GG GGTACC GCTGAGCATGATATGCCAGAAC; Ri 1-R: C GAGCTC TCCTTCCGAACACGAGAAGC.
Ri 2-F: CG ACGCGT TCCTTCCGAACACGAGAAGC; Ri 1-R: CG GGATCC GCTGAGCATGATATGCCAGAAC.
$ config [ads_text16] не е намерен
Амплифицираните фрагменти 1 и 2 се усвояват два пъти с Kpn I/Sac I и Mlu I/BamH I, съответно и след това се клонират в RNAi вектор LH-FAD2-1390. Рекомбинантните плазмиди се трансформират в клетки от суспензия на ориз чрез инфекция с Agrobacterium .
Клетъчна локализация на OsGAS2, OsGrp94 и HSP40 протеини в оризови мезофилни протопласти
За изследването на субклетъчната локализация OsGAS2 (Os01g0276800), OSGrp94 (Os06g0716700) и предполагаемата HSP40 (Os02g0100300) cDNA бяха амплифицирани с генно специфични праймери (BamH I сайт и Kpn I са показани с курсив):
OsGAS2: F-CG GGATCC ATGGGGCTCCACGCGATCC; R-GG GGTACC GCGAGTTCATCATGGTCACGCT.
OsGrp94: F-CG GGATCC ATGCGCAAGTGGGCGCTCTCC; R-GG GGTACC CTACAGCTCGTCCTTATCATA.
HSP40: F-CG GGATCC ATGGATGCTTCTCGCGTTGGC; R-GG GGTACC TTACTGGGACCCATTGAATTT.
PCR продуктите се потвърждават чрез секвениране и след това се пречистват с гел с комплект за екстракция на гел AxyPrep DNA (Axygen, Китай). След това продуктите се усвояват с BamHI и Kpn I и се клонират в субклетъчния вектор за локализация pXZP008 44. Репортерен ген, кодиращ зелен флуоресцентен протеин (GFP), се слива с OsGAS2, OsGrp94 и OsHSP40, който се задвижва от мозаечен вирус на карфиол 35S промотор (35S: OsGAS2/OsGrp94/OsHSP40-GFP) и след това се трансформира и експресира преходно в мезофилен ориз. протопласти. След инкубация в продължение на 16 часа при 26 ° С на тъмно, трансформираните протопласти бяха оцветени с ER-Tracker ™ Blue-White DPX 100 nM (E12353, Molecular Probes, USA) в продължение на 30 минути при 28 ° C на тъмно и измити два пъти с разтвор W5. Флуоресценцията се визуализира с помощта на конфокален микроскоп PerkinElmer UltraVIEW VoX. ER беше идентифициран с помощта на E12353 като контрола.
Експресия и пречистване на рекомбинантен тип A и D 110 A/D 113 Двоен мутант OsGAS2 протеин.
За да се експресира рекомбинантен OsGAS2 в Eschericia coli, пълната дължина на OsGAS2 cDNA (Os01g0276800, WT) и D 110 A/D 113 A мутант (Mu) бяха амплифицирани с помощта на генно специфични праймери (местата Nde I и EcoR I, показани в курсив):
WT: F-GGAATTC CATATG GCCTCCAGGCCGCCGCTCGA;
WT: RG GAATTC TTAGAGTTCAYCATGGTCACG;
D 113 A: F- ACGGGAGTGATGAGTATGCTAGCAATGTCACTTGCAAG
D 113 A: R- CTTGCAAGTGACATTGCTAGCATACTCATCACTCCCGT
D 110 A/D 113: F- TTGCTGCGACGGGAGTGCTGAGTATGCTAGCAATGTC
D 110/D 113 A: R- GACATTGCTAGCATACTCAGCACTCCCGTCGCAGCAA
PCR продуктите, потвърдени чрез секвениране, бяха пречистени с гел и двойно усвоени с Nde I/EcoR I, клонирани в His-tagged pET-28a и след това трансформирани в E. coli DE3. Експресията се индуцира, като се използва 0,3 тМ изопропил-bD-1-тиогалактопиранозид (IPTG) при 37 ° С в продължение на 4 часа. Клетките бяха събрани и ресуспендирани в лизисен буфер (50 mM NaH 2 PO 4 (рН 8.0), 300 mM NaCl). След прекъсване с ултразвук сместа се центрофугира при 10 000 х g за 1 час при 4 ° С. Получената супернатанта се зарежда върху колона със смола Ni-NTA (GenScript, Китай). След измиване на колоната, маркираният с His OsGAS2 се елуира с помощта на елуиращ буфер (50 mM NaH 2 PO 4 (pH 8,0), 300 mM NaCl и 250 mM имидазол).
Разграждане на OsGAS2 чрез активност, подобна на каспаза-3 in vitro
Пречистеният OsGAS2-His 6 протеин (100 μg) се инкубира с каспаза-3 или лизат от цели клетки от термично обработени оризови суспензионни клетки в продължение на 5 часа при 37 ° С в пробен буфер (50 mM HEPES-KOH (рН 7,5), 10% глицерол, 50 mM KCl, 2,5 mM MgCl2 и 1 mM DTT). Разградените продукти се разделят чрез SDS-PAGE и се откриват чрез Western blot, като се използва моноклонално мише анти-поли хистидиново антитяло (разреждане 1: 1000, BOSTER, Китай) като сонда.
Условна експресия на фрагменти от OsGAS2 в протопласти от мезофилен ориз
Фрагменти на OsGAS2: N- и C-фрагментите се амплифицират с помощта на генно-специфични праймери (сайтовете Xho I и Spe I са показани в курсив):
Продуктите се усвояват двукратно с Xho I/Spe I и след това се клонират директно в индуцируем с дексаметазон (Dex) двоичен вектор pTA7002. Получените конструкции и векторната контрола (20–25 μg) бяха трансформирани в протопласти от оризов мезофил.
Анализ на активността като каспаза-3
Протопластите, трансформирани с векторния контрол на pTA7002 или pTA7002-N/C, бяха ресуспендирани в W5 среда (допълнена с 10 mM Dex) и инкубирани в шест ямкови културални плочи при 28 ° C на тъмно за конкретни периоди от време. След инкубация протопластите се третират при 48 ° С в продължение на 15 минути и се оставят да се възстановят при 28 ° С в продължение на 6 часа. Протопластите се суспендират в лизисен буфер (50 mM HEPES (рН 7,4), 100 mM NaCl, 250 mM захароза, 0,1% CHAPS, 1 mM DTT, 0,1 mM EDTA, 1 mg/ml пепстатинин, 8 mg/ml апротинин, 10 mg/mL леупептин). Суспензиите се хомогенизират върху лед и се центрофугират при 12 000 × g за 5 минути при 4 ° С, разтворимите цитозолни фракции се събират и инкубират в пробен буфер (50 mM HEPES-KOH (рН 7,5), 10% глицерол, 50 mM KCl, 2.5 mM MgCl2 и 1 mM DTT), допълнени със 70 mM N-ацетил-Asp-Glu-Val-Asp-7-амино-4-метилкумарин (Ac-DEVD-AMC, EnzoLife Sciences, САЩ). Реакционната система се инкубира без светлина при 30 ° С за 1 h. Флуоресценцията беше измерена в четец за микроплаки (TECAN, САЩ) при 380/460 nm. Разликата във флуоресценцията преди и след инкубацията се нормализира спрямо съответната концентрация на протеин. Всички анализи бяха проведени с помощта на три независими проби.
Електронен микроскоп
Обработените с DTT протопласти се фиксират с 2.5% (w/v) глутаралдехид в CPW-9M (pH 5.8) при 4 ° C за една нощ и след това се фиксират с 1% (w/v) осмиев тетроксид за 3 h при стайна температура. След оцветяване с 1% (w/v) уранил ацетат при стайна температура в продължение на 2 h, протопластите бяха дехидратирани, използвайки няколко различни смеси от етанол, вода и пропиленов оксид, и след това вградени със смола на Spurr. Измерване на участъци
Дебелината от 70 nm се нарязва и се оцветява с уранилацетат и оловен нитрат. Пробните проби бяха наблюдавани с електронен микроскоп (H-7650, Hitachi).
Измерване на съдържанието на цитозолен Ca 2+
Чувствителната към Ca 2+ флуоресцентна боя Fluo-3-AM беше използвана за откриване на относителната промяна на зависимата от Ca 2+ флуоресценция в протопласти. Протопластите бяха инкубирани с 5 μM предварително загрят Fluo-3-AM (Dojindo Laboratories, Япония) в продължение на 30 минути при 37 ° C, както е посочено в инструкциите на производителя. След това клетките се промиват два пъти и отново се суспендират в разтвор на HBSS, съдържащ 0,4 М манитол. Флуоресценцията на Fluo-3 се измерва с конфокален микроскоп PerkinElmer UltraVIEW VoX, използвайки дължини на вълните на възбуждане и емисия съответно 488 и 525 nm. Интензитетът на флуоресценция на протопластите беше измерен чрез ограничаване на отделния протопласт, а средната флуоресценция на протопластите беше измерена и анализирана с Image Pro Plus. За всяко лечение са включени 8–10 протопласта.
Етикетиране на LSD
Протопластите, третирани с DTT и/или 3-MA, бяха събрани и инкубирани с 50 nM LysoTracker Red DND-99 (Molecular Probes, USA) в продължение на 20 минути при 37 ° C, измити с CPW-9M буфер три пъти и след това изследвани от Конфокален микроскоп PerkinElmer Ultra VIEW VoX. Дължината на вълната на възбуждане е 561 nm и емисионните сигнали са измерени при 590 nm.
Коментари
Изпращайки коментар, вие се съгласявате да спазвате нашите Общи условия и разпоредби. Ако откриете нещо злоупотребяващо или което не отговаря на нашите условия или насоки, моля, маркирайте го като неподходящо.
- Garzón обявява нова система за етикетиране за насърчаване на здравословна диета - La Nueva España
- Японската борба се подготвя за евентуалното си завръщане в Superfights
- Черен чай, вашият нов съюзник за отслабване
- Състраданието като цел за новата година
- Ето новата здравословна причина да пиете силно кафе всяка сутрин